

本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分150分.考试时间120分钟.
选 择 题
一、选择题:本题共15小题,每小题4分,共60分.在每小题给出的四个选项中,只有一项是符合题目要求的.
1.在某些恒星内部的核反应中,有下列碳循环反应(简化后):
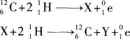
则式中未知原子核X和Y分别为( )
A.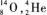
![]()
B.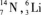
![]()
C.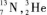
D.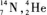
2.一物体以初速度ν0=20 m/s竖直上抛,则物体在4 s内的位移为( )(重力加速度g取10 m/s2.)
A.0
B.10 m
C.20 m
D.40 m
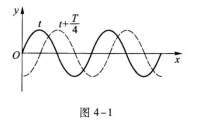
3.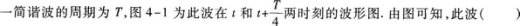
![]()
A.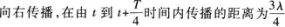
![]()
B.
![]()
C.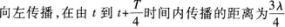
D.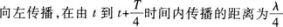
![]()
4.一定质量的理想气体,在体积膨胀过程中,温度不变,则( )
A.气体不吸收热量,内能不变
B.气体不吸收热量,内能减少
C.气体吸收热量,内能增加
D.气体吸收热量,内能不变
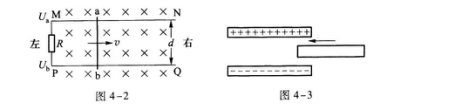
5.如图4-2所示,MN和PQ为两光滑平行导轨,导轨上有一铜棒ab与导轨垂直.导轨处在磁感应强度为B的匀强磁场中,磁场方向与导轨所在平面垂直.当铜棒以一定的速度向右运动时,它所受的安培力为F.若电阻R两端的电势分别为Ua和Ub,则( )
A.F方向向左,Ua<Ub
B.F方向向右,Ua<Ub
C.F方向向左,Ua > Ub
D.F方向向右,Ua > Ub
6.如图4-3所示,有一个平行板电容器,所带的电荷量为Q.在电容器内插入一块厚介质板,插入后电容器上( ) (成人高考更多完整资料免费提供加 微信/QQ:29838818)
A.Q不变,U改变
B.Q不变,U也不变
c.Q改变,U不变
D.Q改变,U也改变
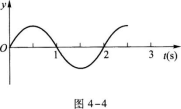
7.图4—4为一质点做简谐运动的振动曲线,则该质点在t=1 s时刻的( )
A.速度为零,加速度为正
B.速度为零,加速度为负
C.加速度为零,速度为负
D.加速度为零,速度为正
8.下列各组物质互为同分异构体的是( )
A.丙烷和2-甲基丙烷
B.2-甲基丙烷和丁烷
C.乙烯和丙烯
D.乙烷和乙烯
9.下列各气体,如果大量排放到空气中,不会造成空气污染的是( )
A.一氧化碳
B.二氧化氮
C.二氧化硫
D.氮气
10.某元素的氢化物的分子式为RH4,其最高氧化物中含氧的质量分数为53%.又知该元素的原子核内质子数等于中子数.则该元素位于周期表的( )
A.第二周期 (成人高考更多完整资料免费提供加 微信/QQ:29838818)
B.ⅡA族
C.ⅣA族
D.ⅥA族
11.下列操作中,选用试剂错误而不能达到目的的是( )
A.实验室干燥NH3气,选用碱石灰(固态NaOH与CaO的混合物)做干燥剂
B.除去Cl2气体中含有的少量HCl气体,用NaOH溶液吸收
C.除去CO2气体中含有的少量HCl气体,用饱和NaHCO3溶液吸收
D.除去C2H6气体中含有的少量C2H4气体,选用Br2水吸收
12.实验室里分别制取下列各组中的气体,可采用同一种气体发生装置制取的气体是( )
A.O2、CO2、H2
B.H2、Cl2、C2H4
C.NH3、CO2、Cl2
D.NH3、CH4、O2
13.下列离子方程式中,正确的是( )
A.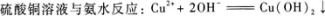
B.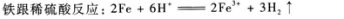
C.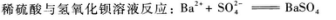
D.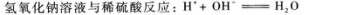
14.有两种金属的混合粉末15 g,加入足量的盐酸,充分反应后,在标准状况下得到11.2 LH2,则下列各组金属中肯定不能构成上述混合物的是( )
A.Mg和A1
B.Mg和Ag
C.Mg和Zn (成人高考更多完整资料免费提供加 微信/QQ:29838818)
D.A1和Fe
15.将0.1 mol/L的NaOH溶液20 mL与0.2 mol/L的CH3COOH溶液10 mL混合.混合后的溶液中,有关离子浓度间的关系正确的是( )
A.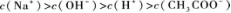
B.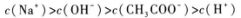
C.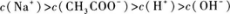
![]()
D.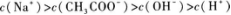
非选择题
二、填空题:16~19题每题6分,20~28题每空3分,共57分,把正确答案填在题中横线上.
16.

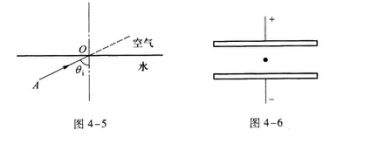
17.如图4-6所示,两金属板间有一匀强电场,场强大小为E,方向竖直向下.其中有一油滴,质量为m,带负电2q,具有向下的加速度a;如果是一质量相同的带负电3q的油滴,则具有向
18.一质量为m的重锤从高为h处自由落下,陷入地面的深度为s.在陷入地面的过程中,重力对锤所做的功为 ;阻力对锤所做的功为 .(重力加速度为g.)
19.如图4—7所示,矩形区域ABCD内有一磁感应强度为B的匀强磁场,磁场内有一长为l1,宽为l2,电阻为R的小矩形线框abcd,线框平面与磁场垂直,cd边和CD边互相平行.若使线框沿其平面以垂直cd边的速度ν平移出磁场,则线框中感应电流持续的时间t为 ;电流的大小为 ,方向为 .(填“顺时针”或“逆时针”.)
20.禁止用工业酒精兑制饮用酒,是因为工业酒精中含有少量使人致盲、致死的有毒物质,该物质是 .
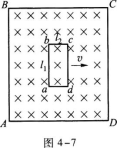
21.某有机物的氧化产物A和还原产物B,都能与金属钠反应放出氢气,A与B反应生成C4H8O2.该有机物的名称是 .
22.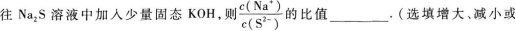
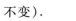
![]()
23.标准状况下,7 g某气体与0.5 g氢气所含的分子数目相同,则该气体的密度(标准状况下)为 g/L
24.
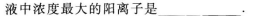
![]()
25.常温下,物质的量浓度相同的NaHSO4、NH4HSO4、NaHCO3三种溶液,其pH从小到大的顺序依次为 .
26.一种无色溶液可能含有KNO3、NH4Cl、Na2SO4、(NH4)2SO4、Na2CO3、(NH4)2CO 3中的一种或几种,用其做如下实验,现象是:
(1)取少许溶液进行焰色反应,透过蓝色钴玻璃观察,火焰呈浅紫色.
(2)往溶液中加入少量NaOH溶液并加热,产生有刺激性气味的气体.
(3)往溶液中加入少量BaCl2溶液,有白色沉淀生成.继续加入过量稀HNO3,白色沉淀部分溶解.试判断溶液中一定含有的物质是 ;白色沉淀溶于稀HNO3的离子方程式是 .
27.

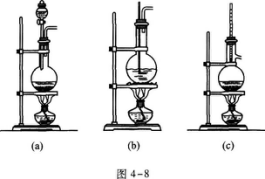
28.实验室中用乙醇制取乙烯时,采用的气体制备装置是图4—8中的 (填图下的符号).
三、计算题:本题共3小题,共33分.解答时要求写出必要的文字说明、方程式和重要的演算步骤.只写出最后答案而未写出主要演算过程的,不能得分.
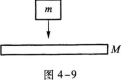
29.(本题11分)如图4-9所示,在光滑水平地面上,一质量为M的物体以ν0的速度做匀速直线运动.把另一质量为m的物体轻放在M上,由于m与M间的摩擦作用,经时间t后两者以共同速度运动.求:
(1)两物体共同运动速度的大小ν;
(2)在时间t内,m所受摩擦力的大小.
30.(本题12分)如图4—10为一分压电路,它为R0=20 Ω的负载电阻提供可变的电压.已知电源电动势ξ=6 V,内阻r=1 Ω;AB为滑线变阻器,总阻值R=10 Ω.求:
(1)滑片P与A端接触时电压表的读数;
(2)滑片P与AB的中点接触时电压表的读数.
31.(本题10分)在含有Na2SO4和Na2CO3的0.5 L溶液中,加入足量BaCl2溶液,生成沉淀4.3 g.过滤后向沉淀中加入足量稀HNO3,则可得到224 mL(标准状况下)的气体.计算
(1)原溶液中含Na2CO3的质量.
(2)原溶液中Na2SO4的物质的量浓度.
物理化学模拟试卷(四)参考答案及解题指要
选择题
一、选择题 (成人高考更多完整资料免费提供加 微信/QQ:29838818)
1.【参考答案】 D
【解题指要】 本题考查的知识点是平衡核反应方程,基本规律是原子核反应过程中电荷数守恒和核子数守恒(前者表示电荷守恒,后者表示质量守恒).平衡核反应方程的步骤是根据反应前后核子数相等的规律,求出未知原子核的质量数A,再根据反应前后电荷数相等求得未知核的电荷数Z.最后由Z确定未知核的元素符号,写出所求的原子核.
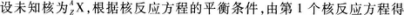
12+2=A+0
6+2=Z+1
由此得
A=14. Z=7

2.【参考答案】 A
【解题指要】 本题考查的知识点是竖直上抛运动,竖直上抛运动是匀减速直线运动.
已知初速度ν0,求t时的位移,因此用竖直上抛运动的位移公式解题.竖直上抛运动的位移公式是
![]()
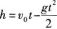
代人题给数值算得
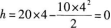
故选A.
在本题所给的数据下,竖直上抛运动的上升时间为

可见4 s正好是物体的落地时间.显然物体落地时的位移为零,有些考生据此直接选A.注意,这只是本题所给条件下的特例,建议考生还是直接用位移公式求解,不易失误.
3.【参考答案】 B
【解题指要】 本题考查的知识点是波形图.从静态来看,波形图是指某一时刻的波形.从动态来看,在波传播的过程中,波形图沿波的传播方向行进.简谐波的波形图以速度ν沿波的传播方向前进,只要从图中判断波形图的前进方向就可以确定波的传播方向.

4.【参考答案】 D (成人高考更多完整资料免费提供加 微信/QQ:29838818)
【解题指要】 本题考查的知识点是气体的功、理想气体的内能以及内能与功、热传递的关系.气体的功与它的体积有关.当气体膨胀时,体积增加,气体对外界做功;当气体压缩时,体积减小,外界对气体做功.一定质量的理想气体的内能决定于它的温度,温度上升内能增加,温度下降内能减少,温度不变内能不变.按题意知,一定质量的理想气体经历了等温膨胀过程,体积增大,温度不变.因此,气体对外界做功,内能不变,排除B、C.根据内能与功和热传递的关系知,当气体对外做功时内能要减小,只有同时吸热的情形下才能保持内能不变,故选D.
5.【参考答案】 C
【解题指要】 本题考查的基本规律是:感应电动势、右手定则、磁场对通电导线的作用力、左手定则.铜棒在磁场中切割磁感线时产生了感应电动势,感应电动势的方向由右手定则确定.通电的铜棒在磁场中受到磁场力的作用(安培力),磁场力的方向由左手定则确定.由右手定则知,ab上感应电动势的方向(即ab上感应电流的方向)由b→a,这表明a点的电势比b点的电势高,Ua>Ub,排除A、B.再用左手定则,可以判断磁场力Fm的方向向左,故选C.在用右手定则判断感应电动势时,必须注意在ab上感应电动势的方向是由低电势指向高电势的.有的考生因为感应电流由b向a而误判Ub>Ua.其实,只有在外电路中电流是由高电势处流向低电势处,在电源中则是由低电势处流向高电势处.铜棒ab是闭合电路中的电源,棒中的电流是由低电势流向高电势的,即Ua>Ub.解本题时需要同时应用左手定则和右手定则.必须注意两者的区别,切勿混淆.左手定则表示“电、磁、力”的关系,右手定则表示“电、磁、动”的关系,如图4-11所示.
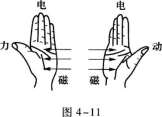
6.【参考答案】 A
【解题指要】 本题的考点是电容器电容的大小与介质的关系以及电容器公式.
我们知道,当平行板电容器中插入介质板后可以使电容C增大.此外,由图4-3知,平行板电容器充电后未接电源,所以它所带的电荷量Q不会改变.根据电容器公式
![]()
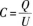
知,在Q不变时,U与C成反比.因此C增大则U减小,故选A.
请考生思考:平行板电容器中插入介质块后,电容器中的电场强度E是否改变?
7.【参考答案】 C
【解题指要】 本题考查的知识点是简谐运动的图像和简谐运动的基本过程.
题意是给出振动曲线,要求判断质点某时刻的运动情况.由振动曲线可知,质点在t:0时由平衡位置开始沿y轴正方向做简谐运动,它在t=1 s时振动了半周回到平衡位置,然后沿y轴负方向运动,到t=2 s时完成了一个全振动过程,回到平衡位置,继后周而复始地运动.当质点做简谐运动时,在端点时的速度为零,然后向平衡位置方向运动,速度增大,在平衡位置时速度最大.质点在端点时位移最大,弹力最大,加速度也最大;质点在平衡位置时,位移为零,弹力为零,加速度等于零.t=1 s时质点位于平衡位置,加速度为零,排除A、B.质点沿y轴负方向运动,所以速度为负,故选C.在振动曲线上,曲线上某点的切线方向表示该点的运动方向.显然在t=1 s点,切线的方向斜向下,所以速度是负的.
8.【参考答案】 B
【解题指要】 正确解答此题,首先必须准确地掌握同分异构体的概念,即只有分子式相同、结构不同的有机物,才互称同分异构体.其次,应能根据有机物的名称,写出正确的结构简式和分子式.本题中涉及的有机物有乙烷、乙烯、丙烯、丙烷、丁烷和2-甲基丙烷6种,它们的结构简式和分子式分别是:



由此可知,丁烷和2-甲基丙烷互为同分异构体,即8选项正确.
9.【参考答案】 D
【解题指要】 CO有剧毒,能严重危害人体健康.人若吸人少量CO会感到头痛,吸入较多量CO就会因缺乏氧气而死亡.所以CO是大气的主要污染物之一.NO2是一种有毒气体,是造成光化学烟雾的主要因素.光化学烟雾刺激呼吸器官,使人生病甚至死亡.NO2也是形成酸雨的原因之一.SO2也是一种有毒气体,它对人体的直接危害是引起呼吸道疾病,严重时还会使人死亡.另外,空气中的SO2在氧气和水的共同作用下,会形成酸雾,进而形成酸雨.所以SO2是污染大气的主要有害物质之一.N2是空气的主要成分之一,在空气中的含量达到78%之多,一般不会造成对大气的污染.
10.【参考答案】 C
【解题指要】 (1)要想知道元素在周期表中的位置,需知道元素的原子序数.由氢化物的分子式RH4可知,其最高价氧化物的分子式为RO2.设R的原子质量数为x,则

11.【参考答案】 B
【解题指要】 除杂质的试剂(或干燥剂)应与杂质(或水)反应,生成能与主要成分分离开来的生成物,而不能与主要成分发生化学反应.
A选项正确.因水蒸气可被固态NaOH吸收,也可与CaO发生如下反应:
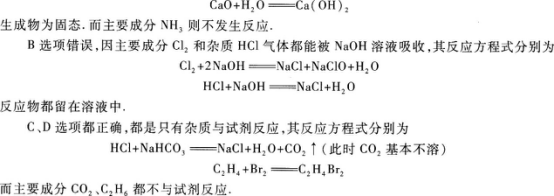
12.【参考答案】 D
【解题指要】 解答此题主要考虑两个条件:
①制取气体的反应类型要相同.如“固+固→气”与“固+液→气”,其反应类型不同,采用的制取装置也不可能相同.
②反应条件要相同.如“固+液→气”这一类型中,有加热和不加热之分.反应条件不同,采用的制取装置也不可能相同.
在D选项中,制取NH3、CH4、O2都属于“固+固→气”一类,且均需加热.所以D选项正确.
13.【参考答案】 D
【解题指要】 A选项中氨水为弱电解质,正确的离子方程式为

14.【参考答案】 A
【解题指要】 (1)Mg、Fe、Zn与盐酸反应均呈+2价,只有A1与盐酸反应时呈+3价,但A1与盐酸反应生成1 molH2时,需A1的质量为
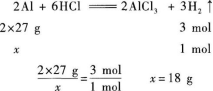
(2)设金属混合物的平均相对原子质量为y(金属均按2价计算),则
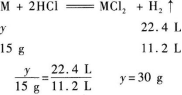
即混合物的平均相对原子质量为30.
(3)由两种金属组成的混合物且其平均相对原子质量为30,则其中必有一种金属的相对原子质量大于30,另一种金属的相对原子质量小于30.C选项,Mg为24,Zn为65.D选项,A1看做+2价时,其相对原子质量为18;Fe为56.所以C、D选项均可.A选项,Mg为24,A1为18(+2价时),都小于30,所以A选项是不可能的.B选项,虽然Ag不与盐酸反应,但因Mg可与盐酸反应放出H2,且Mg的相对原子质量小于30,所以Ag与Mg组成的混合物也符合要求.
15.【参考答案】 D
【解题指要】 溶液中含有NaOH和CH3COOH的物质的量分别为
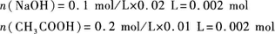

非选择题
二、填空题
16.【参考答案】 如图4—12所示
【解题指要】 本题的考点是光的反射定律、折射定律和光的全反射.
当光从一种介质射到另一种介质时,一束入射光在介质的分界面通常会分成反射光和折射光两束.反射光线满足反射定律,折射光线遵从折射定律.由反射定律知,反射角等于入射角,由此立即可以画出反射光线,如图4一12所示.

解题时先不必急于面出折射光线,而首先仔细分析题意,由题意知,光是从水射向空气,水相对空气而言是光密介质,因此本题是由光密介质射向光疏介质的情形,在这种情形下要注意可能发生全反射.当入射光由光密介质射人光疏介质时,只要入射角大于全反射的临界角,则发生全反射现象,没有折射光线.光从介质射入空气时全反射的临界角是
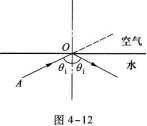
由此可知θi>θc
显然在本题的条件下发生全反射,无折射光线.
有些考生没有仔细分析题意,直接用折射定律求折射角,根据折射定律知

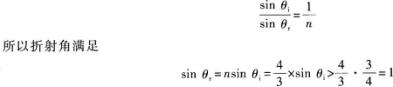
![]()
17.
![]()
【解题指要】 本题是静电学和动力学结合的试题,考查的知识点是电场力和牛顿第二定律.
先分析第一种情形.负电荷受到向上的电场力Fe的作用,重力G竖直向下.G大于Fe所以合外力向下,加速度向下.
电荷所受的电场力为
Fe=2qE
重力为 G=mg
取竖直向下为正方向,则合外力为
F=mg-2qE
由牛顿第二定律知
mg一2qE=ma ①
再分析第二种情形.已知此情形下加速度向上,所以电场力Fe大于重力G.取竖直向上为正方向,写出牛顿方程有
Fe一G=ma
把 Fe=3qE
代入上式得
3qE—mg=ma ②
由式①、②得


18.【参考答案】mgs -mg(h+s)
【解题指要】 本题的考点是重力的功、阻力的功、动能定理.
解本题最简捷的方法是对重锤开始下落到陷入地面的全过程用动能定理.在整个过程中只有重力和阻力做功,重力做正功,阻力做负功.

有的考生把全过程分成两个过程考虑,第一个过程是重锤做自由落体运动,第二个过程是重锤陷入地面中,然后再对两个过程分别用动能定理解题.在第一个过程中只有重力做功;在第二个过程中重力做正功,阻力做负功.这样的解题方法比较麻烦,容易造成失误.此外,必须注意题意求陷入地面过程中重力的功,而不是全过程中重力的功,有的考生在第一个空格中误答为mg(h+s).
19.
![]()
【解题指要】 本题是力学、电学综合试题.考查的知识点有:匀速直线运动、电磁感应定律、感应电动势、闭合电路欧姆定律和右手定则.
在图示的位置中,虽然线圈在运动,但是ba、cd两边上感应电动势的大小相等、方向相反,相互抵消,线圈的感应电动势为零,无感应电流.从整个线圈来看,通过线圈的磁通量不变,由法拉第电磁感应定律知,线圈的感应电流为零.当cd边开始离开磁场时,cd上无感应电动势,但ba边上有感应电动势,线圈的感应电动势就等于ba上的感应电动势,所以线圈中有感应电流.或者从整个线圈来看,随着cd边离开磁场,通过线圈的磁通量减小,因此根据法拉第电磁感应定律知线圈中有感应电流.显然当ba边离开磁场时,整个线圈全部离开磁场,线圈上不再有电流了.因此线圈中电流持续的时间为从cd离开磁场开始到ba也离开磁场为止.这段时间内线圈平动的距离为bc的长度l2,速度为ν,因此电流持续的时间为
![]()
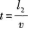
根据闭合电路的欧姆定律,感应电流的大小为
![]()
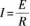
由感应电动势公式知
![]()
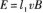

用右手定则可以确定ba上感应电动势的方向由a指向b,因此线圈中感应电流的流向为abcda,即顺时针方向.
20.【参考答案】 甲醇
【解题指要】 工业酒精中含有一定量的甲醇,所以工业酒精不能饮用.此题不要求解释为什么,所以只要记住甲醇即可.
21.【参考答案】 乙醛
【解题指要】 (1)在《考试大纲》的范围内.能与金属钠反应生成H2的有机物有乙醇和乙酸.
(2)有机物的还原产物B和氧化产物A都能与金属钠反应.说明该有机物一定是醛类物质,其氧化产物为酸,还原产物为醇.
(3)根据A、B反应生成C4H8O2,说明该有机物为乙醛,因为氧化、还原过程中碳原子数是不变的,其反应方程式为
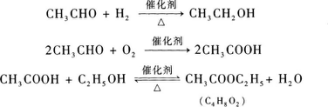
所以该有机物是乙醛.
22.【参考答案】减小
【解题指要】 (1)在Na2S溶液中
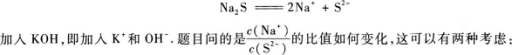

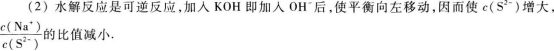

23.【参考答案】1.25
【解题指要】 (1)要求得某气体的密度,就应知道该气体的质量和该质量的气体所占有的体积.由题目已知气体质量是7 g,还要求得7 g气体在标准状况下所占有的体积.
(2)根据“7 g某气体与0.5 g氢气所含的分子数目相同”,就是说它们的物质的量相同.因


